Hay una relación simple entre el trabajo mecánico realizado en un sistema y el calor generado en él. James Prescott Joule encontró por primera vez experimentalmente que el calor producido en un sistema es directamente proporcional al trabajo mecánico realizado en él. También calculó la constante de proporcionalidad a través de un experimento único, que también describiremos en este artículo. La constante es conocida popularmente como Equivalente mecánico del calor. Después del nombre de James Prescott Joulela constante también se conoce como Jules Equivalente Mecánico del Calor o simplemente Constante de Jules. Lo designamos con la letra J mayúscula en inglés.
 Si W es el trabajo realizado en un sistema y Q es la cantidad de calor producida debido a este trabajo, entonces
Si W es el trabajo realizado en un sistema y Q es la cantidad de calor producida debido a este trabajo, entonces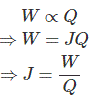
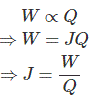
La expresión de J dice que, el equivalente mecánico del calor es el número de unidades de trabajo, que debe hacerse en un sistema para producir una sola unidad de calor.
Experimento de Jules


Para demostrar su experimento, primero tomaremos un calorímetro cilíndrico hecho de cobre.

Usaremos un sistema de paletas como se muestra arriba.

Ahora, llenaremos el calorímetro con una cantidad definida de agua. Ahora uniremos el sistema de paletas al calorímetro lleno de agua con una cubierta superior hermética.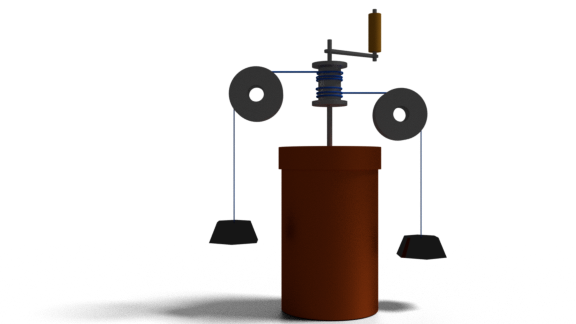

Ahora, adjuntaremos dos pesos de masa conocida e igual como se muestra en la figura de arriba, con la ayuda de poleas. Cuando giramos el mango del sistema en cualquier dirección, ambas pesas suben o bajan verticalmente dependiendo de la dirección de rotación.

Adjuntamos dos escalas verticales para medir la vertical; movimientos de los pesos. También colocamos un termómetro en la cubierta superior del sistema para ver el aumento de la temperatura del agua.

Ahora levantaremos las pesas girando el mango. Después de levantar las pesas por la altura h dejamos que caigan libremente a sus posiciones anteriores. Cuando las pesas caen, la energía potencial almacenada en el sistema durante el levantamiento de las pesas, se libera como energía cinética que causa la rotación de las camionetas en el agua. Este trabajo realizado en el sistema, generará calor en el agua y causa el aumento de la temperatura del agua. Después de que las pesas bajen a su posición de descanso, de nuevo, levantaremos la pesa para la misma altura h y permitiremos que éstas bajen libremente. Continuamos haciendo esto hasta que haya una diferencia de temperatura medible indicada en el termómetro instalado en el sistema.
Ahora, podemos medir el trabajo realizado multiplicando el peso total por el movimiento de la altura de los pesos, el número de veces que los movimientos de los pesos se repiten.
Consideremos que ambos pesos tienen la misma masa m. Por lo tanto, la masa total de los pesos es de 2m. Por lo tanto, el trabajo realizado debido a la caída de las pesas verticalmente por h metros es 2mgh. Ahora digamos, total de n repeticiones de los movimientos de las pesas hechos antes de elevar la temperatura del agua a su valor medido. Por lo tanto, el trabajo total realizado será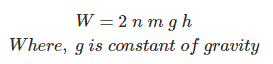
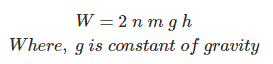
Aquí se conocen todas las n, m, g y h, por lo que el trabajo total realizado puede ser fácilmente calculado.
Consideremos ahora que M es la masa de agua en el calorímetro. W es el equivalente en agua del calorímetro.
Así que el calor total producido por el aumento de la temperatura del agua es,![]()
![]() Q = (M + W).
Q = (M + W).
Ahora, el equivalente mecánico del calor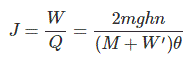
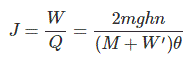
Después de este experimento, poniendo todos los valores conocidos de m, g, h, n, M, W y , obtenemos,![]()
![]()
Aquí, en este experimento, la energía potencial de la masa descendente se convierte en la energía cinética y finalmente en la energía calorífica.