Los fundamentos de la termodinámica de la ingeniería juegan un papel importante en el avance hacia un mundo mejor, a través de la mejora del rendimiento de la planta, el equipo y su diseño general.
Los factores que son críticos para evaluar el rendimiento del equipo son elementos como la producción del producto final, el consumo de materia prima de entrada, el costo de producción y la evaluación del efecto sobre el medio ambiente. Los ingenieros de hoy en día están utilizando el concepto de termodinámica para examinar y reinventar cosas que están destinadas a la seguridad y comodidad humanas.
La ciencia de la termodinámica ha existido desde el 19th siglo. Desde entonces, los científicos e ingenieros han hecho un esfuerzo constante y continuo para que sea lo más fácil de usar posible.
Fundamentos de la termodinámica
La palabra termodinámica se deriva de la palabra griega theme (significa calor) y dynamics (significa fuerza). Los profesionales de la ingeniería están interesados en el estudio de los sistemas y su interacción con el entorno.
Los conceptos/definiciones utilizados en esta sección son útiles para que los lectores comprendan el concepto de termodinámica de ingeniería (a veces denominada Ingeniería de Potencia Calórica)
Sistema, entorno y universo
Un sistema es algo que queremos estudiar e interesar, por lo que el primer paso es fijar con precisión el objetivo del estudio del sistema. El objetivo del estudio del sistema puede ser mejorar la eficiencia del sistema o reducir las pérdidas, etc. Ejemplo de sistema puede ser analizar el ciclo de refrigeración en una planta de almacenamiento en frío o analizar el Ciclo de Rankine en planta de energía.
Un sistema se define como una masa definida de sustancia pura delimitada por una superficie cerrada o flexible; del mismo modo, la composición de la materia en el interior del sistema puede ser fija o variable según el ciclo.
Las dimensiones del sistema no son necesariamente constantes (como el aire de un compresor es comprimido por un pistón) puede ser variable (como un globo inflado). La materia que interactúa con el sistema externamente se llama «Alrededor» y el Universo es el resultado del sistema y sus alrededores.
El elemento que separa el sistema de su entorno se llama límite. El límite del sistema puede ser fijo o en movimiento.
La interacción entre el sistema y el entorno tiene lugar al cruzar la frontera y, por lo tanto, desempeña un papel muy importante en la termodinámica (es decir, la ingeniería del calor y la energía).
Tipos de sistema en la termodinámica
Hay dos tipos básicos de sistemas en la termodinámica:
- Sistema cerrado o masa de control: se asocia con la cantidad definitiva de hombre ater. A diferencia de un sistema abierto, en un sistema cerrado no hay flujo de masa de materia que se produzca a través de los límites del sistema. También existe un tipo especial de sistema cerrado que no interactúa y se aísla del entorno se denomina sistema aislado.


- Control de volumen (sistema abierto): El volumen de control se limita a una región del espacio a través de la cual la masa y la energía pueden fluir y cruzar el límite del sistema. El límite de un sistema abierto se denomina superficie controlada; esta superficie controlada puede ser real o irreal.
Ejemplos de volumen de control son los tipos de equipo que implican el flujo de masa para cruzar el límite del sistema, como el flujo de agua a través de bombas, vapor el flujo en las turbinas y el flujo de aire a través de los compresores de aire.
Termodinámica microscópica
El enfoque microscópico en termodinámica también se llama termodinámica estadística y se asocia con la estructura de la materia y el objetivo de la termodinámica estadística es caracterizar el comportamiento promedio de la partícula que compone el sistema de interés y, a su vez, utilizar esta información para observar el comportamiento macroscópico del sistema.
Propiedad, estados y proceso de la termodinámica
Propiedad termodinámica
Una propiedad termodinámica es una característica macroscópica de un sistema. El valor de una propiedad puede ser asignado en cualquier momento sin el conocimiento del valor previo y su comportamiento.
Propiedad extensiva
Las propiedades que dependen de la masa se denominan propiedades extensivas y su valor para el sistema global es la suma de sus valores para las partes en las que se divide el sistema. Ejemplos de propiedades extensivas son el volumen, la energía y la masa. La propiedad extensiva depende del tamaño de un sistema y puede cambiar con el tiempo.
Propiedad intensiva
A diferencia de la propiedad extensiva, la propiedad intensiva no depende de la masa ni de la naturaleza aditiva y no depende del tamaño total del sistema. Puede variar en diferentes lugares del sistema en cualquier momento. Ejemplos de la propiedad intensiva son la presión y la temperatura.
Estado termodinámico
Un estado se define como la condición de un sistema que se describe mejor por sus propiedades. La masa encerrada en un sistema puede encontrarse en una variedad de condiciones únicas, llamadas estado. Hay relaciones entre las propiedades de un sistema pero el estado puede especificarse proporcionando el valor de un subconjunto de las propiedades.
Proceso termodinámico
Los procesos termodinámicos son la conversión de un estado a otro estado. Si el valor de la propiedad macroscópica del en un sistema en dos momentos diferentes son idénticos, entonces se dice que el sistema está en un mismo estado en ese momento. La condición de estado constante del sistema se logra si ninguna de sus propiedades cambia con respecto al tiempo.
Ciclo del equilibrio del sistema
A sistema termodinámico El ciclo de equilibrio es un proceso secuencial que comienza y termina con la condición del mismo estado. Cuando el ciclo se completa, entonces todas sus propiedades tienen el mismo valor que tenían al principio. Todos los ciclos que se repiten regularmente juegan un papel vital en muchas áreas de aplicación, como la circulación de condensado en un estación de generación de energía térmica ejecuta un ciclo.
Sustancia de trabajo
La teoría de la materia es útil para comprender el concepto de energía. La materia es conocida por su masa, volumen y espacio e independientemente de su estructura y naturaleza tiene ciertas características como la consistencia y la fiabilidad. La materia está hecha de un gran número de partículas llamadas moléculas. Se pueden encontrar materias sólidas, líquidas o gaseosas en todas partes.
En la materia sólida, las moléculas están cercanas entre sí y fuertemente ligadas y no pueden moverse libremente. Por lo tanto, se requiere una gran fuerza para cambiar su forma.
Las moléculas de una materia líquida no están firmemente sujetas y, por lo tanto, una fuerza muy pequeña es suficiente para mantener las moléculas juntas.
En estado gaseoso las moléculas se mueven aleatoriamente y libremente como si estuviera en un estado no ligado entonces se mueve muy rápido independientemente de sus moléculas adyacentes. La compresibilidad se asocia a los gases, tienen muchos espacios vacíos entre las moléculas que se conectan. La energía es la razón de que la materia exista en diferentes fases.
Sustancia pura
El material de estructura química única o de homogeneidad en la estructura química variante se conoce como sustancias puras. Los materiales pueden existir en una sola fase como el líquido o también pueden existir en más de una fase en equilibrio entre sí. Una mezcla uniforme de gases de composición química similar también se denomina sustancia pura.
La importancia de la sustancia pura radica en la determinación de las propiedades de la sustancia de trabajo en diferentes condiciones de presión y temperatura.
Ejemplo:Para una sustancia pura como el agua puede describirse plenamente por dos propiedades intensivas soberanas denominadas presión y temperatura. Otra sustancia pura es el aire en estado gaseoso. Pero para una sustancia no homogénea, se requieren más de dos propiedades para describir el estado.
Equilibrio termodinámico
En la mecánica, se dice que el equilibrio se alcanza cuando igualamos las fuerzas opuestas. Pero el significado de equilibrio termodinámico es diferente y de gran alcance, ya que implica un acto de equilibrio para muchas otras influencias (entre y el sistema y el entorno) además de equilibrar las fuerzas opuestas). Para alcanzar el equilibrio completo con en un sistema, es necesario cumplir la condición de equilibrio mecánico, térmico, de fase y químico.
En esta sección, limitamos nuestra discusión al equilibrio termodinámico. El énfasis en tener estados de equilibrio y su cambio de un equilibrio a otro se describe mejor en la Termodinámica Clásica.
Si el estado es fijo, entonces se dice que el sistema está en equilibrio. Propiedades intensivas como la presión y la temperatura deben ser medidas con precisión para asignar el estado. Se dice que un sistema está en equilibrio termodinámico si sus propiedades intensivas no cambian a causa de muy poca perturbación.
En esta situación, el sistema está en completa estabilidad con las restricciones que ofrece el entorno.
Proceso de equilibrio real y cuasi-equilibrio
Durante un proceso real, el asistema puede considerarse como no equilibrado debido a los diversos efectos de no equilibrio presentes en el sistema y, por lo tanto, muestra un cambio en la presión y la temperatura.
En el proceso de cuasi-equilibrio (cuasi-estático) la desviación del estado de equilibrio termodinámico es extremadamente pequeña. Por lo tanto, todos los estados por los que pasa el sistema se consideran en estado de equilibrio durante un proceso de cuasi equilibrio.
El cuasi-equilibrio se utiliza para derivar relaciones entre varias propiedades extensas como la entropía, la energía interna, los calores específicos y entalpía etc.
Dimensiones y unidades
La cantidad física se conoce por sus dimensiones y si se le da la magnitud a esta dimensión entonces se denomina unidad. El requisito previo de los cálculos de ingeniería es tener la misma unidad de cantidades físicas.
Algunas dimensiones vitales como la masa (m), la longitud (L), el tiempo (t) y la temperatura (T) se denominan dimensiones primarias. Ingenieros y científicos de todo el mundo están realizando sus cálculos principalmente en dos tipos de unidades llamadas el sistema inglés y el sistema métrico (SI). Sistema de unidad del SI La representación es más lógica y comúnmente utilizada por los profesionales.
| Dimensiones primarias | Unidad métrica (SI) | Unidad de Inglés |
| Longitud | Metros (m) | Pie (ft) |
| Masa | Kilogramo (kg) | Libra (lb) |
| Tiempo | Segundos (s) | Segundos (s) |
| Temperatura | Kelvin (K) | Fahrenheit |
| Corriente eléctrica | amperios (A) | amperios (A) |
Dimensiones y unidades secundarias
Las dimensiones secundarias o derivadas se expresan en términos de dimensiones primarias como Velocidad (V), Energía (E), y Volumen (V), Fuerza, Potencia, Calor, etc.
La fuerza se considera una dimensión secundaria en las unidades del SI, ya que su unidad se deriva de la segunda ley de Newtons que es![]()
![]()
La fuerza se define como la fuerza necesaria para acelerar una masa de 1 kg a una velocidad de 1 m/s2.
El peso y la masa no deben ser considerados como lo mismo. El peso es la fuerza gravitatoria que actúa sobre un cuerpo y su magnitud se determina a partir de la segunda ley de Newtons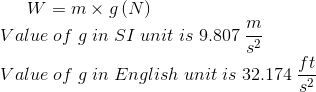
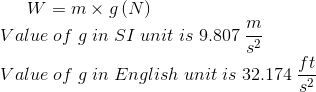
El peso específico (y) se define como la fuerza de gravedad que actúa sobre un volumen unitario de una sustancia y se determina por y = (densidad ) g N/ m3
Así, independientemente de la ubicación en el universo, la masa del cuerpo sigue siendo la misma. Cuando la aceleración gravitatoria cambia, el peso del cuerpo también cambia. En la cima de la montaña, el cuerpo pesa menos, ya que su peso disminuye con la altitud.
El Volumen Específico() y la Densidad() son propiedades intensivas y pueden diferir de un punto a otro. La densidad recíproca es un volumen específico.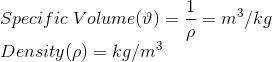
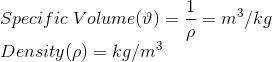
La presión: La presión se define como una fuerza normal ejercida por un fluido por unidad de superficie en caso de líquido o gas. En el caso de los sólidos, la presión es equivalente a la tensión normal.
Unidad SI de presión y estrés es Pascal (N/ m2). A continuación se indican otras unidades de presión:
| 1 Pascal | 1 N/ m2 |
| 1 K Pascal | 103 N/ m2 |
| 1 barra | 105 N / m2 |
| 1 M Pascal | 106 N/ m2 |
| 1 atm | 101.325 kpa=1.01325 barras |
| 1 Bar | 100 kpa = 0.1 M Pascal |
| 1 kgf/cm2 | 9.807 N/cm2 = 0.9807 Bar = 0.9679 atm |
La presión absoluta está relacionada con la presión real en un punto determinado y la medición se realiza con respecto al vacío absoluto o la presión cero absoluta.
La presión real en un punto determinado se denomina presión absoluta y se mide en relación con el vacío absoluto (presión cero absoluta).
Las presiones por debajo de la presión atmosférica se denominan Presión de vacío y se miden mediante un vacuómetro que indica la diferencia entre la presión atmosférica y la presión absoluta.

La figura anterior describe mejor la relación entre la presión absoluta, la presión atmosférica, la presión manométrica y las presiones de vacío
Energía y formas de energía
La energía se define como la capacidad de hacer el trabajo. La entrada de energía siempre produce algún efecto en la materia del sistema.
Dos tipos principales de energía son: Energía almacenada y energía en tránsito
- En la materia la energía almacenada puede salir en varias formas como Energía Interna (IE), Energía Cinética (KE), Energía Potencial (PE), Energía Química (CE), Energía Eléctrica (EE), Energía Nuclear (NE). Los detalles de esta energía se discutirán en la siguiente sección.
- Energía en tránsito
Calor
El calor se define como la energía transferida sin la transferencia de masa a través del límite de un sistema debido a la diferencia de temperatura entre el sistema y los alrededores. La energía en transición sola se llama calor. La cantidad de calor transferida durante un proceso depende del camino seguido y no sólo de las condiciones finales.
Trabajo

Cuando la fuerza F se utiliza para mover una o más partículas a través de una distancia x entonces se llama Trabajo. En una disposición de cilindros de pistón inferior dada para disminuir el volumen V de un sistema, se requiere que se trabaje. Por lo tanto, en un volumen extremadamente pequeño el cambio en el sistema como resultado del movimiento del pistón está relacionado con el diferencial en el trabajo a través del producto fuerza-distancia por la fórmula:
dW = Fdx = pAdx = pdV [ ft-ldf | Nm] .. (1)
dw = pdv [Btu / lbm | KJ/kg ] .. (2)
Donde, p es la presión del sistema, A es el área, F es la fuerza, x es la distancia incremental recorrida, W es el trabajo, V es el volumen
Las letras minúsculas en la ecuación 1 y 2 son para el trabajo y el volumen basado en la masa por unidad. Las propiedades extensas con caracteres en minúscula se llaman propiedades específicas.
La ecuación 1 está en unidad inglesa, mientras que la unidad térmica británica (BTU) se utiliza en la ecuación 2 y los dos conjuntos de unidades están vinculados por un factor de conversión llamado Mecánico-Equivalente de calor y su valor es 778 ft-lbf / Btu.



